Réactions et mécanismes avec les amines
La réactivité des amines provient de la polarisation due à l'électronégativite de l'azote.
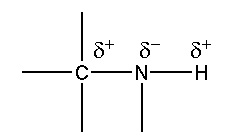
L'électronégativite de l'azote est plus faible que celle de l'oxygène. La polarisation sera donc moins importante que dans le cas des alcools.
La présence du doublet non liant sur l'atome d'azote rend les molécules basiques et de bons nucléophiles. Celui-ci lui confère également une géométrie en tétraèdre. Elles peuvent facilement se protoner.
Les substituants vont accentuer ou diminuer cette basicité. Si le groupement a un effet inductif attracteur, le caractère basique de l'amine est diminué (COOH par exemple). A l'inverse, un groupement donneure tel que -CH3 accentue la basicité. A noter que les amines tertiaires sont souvent moins basiques que les primaires et secondaires en raison de l'encombrement stérique.
La plupart de ces composés sont liquides à températures ambiantes.
Caractère nucléophile
Le caractère nucléophile permet les réactions d'alkylation avec substitution sur un dérivé halogéné. Les réactions d'Hoffman utilisent cette propriété.
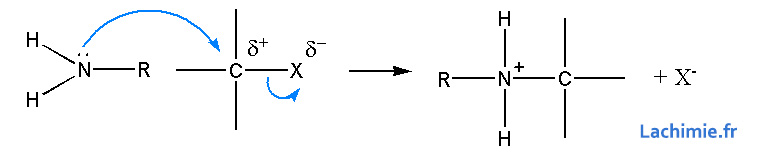
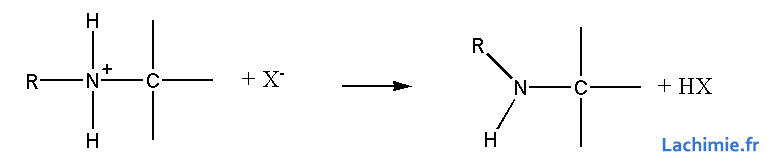
L'ammonium formé n'est qu'un intermédiaire de réaction. Il continu a réagir sur le composé halogéné jusqu'à la formation d'un ammonium quaternaire qui lui est stable.
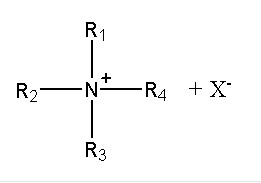
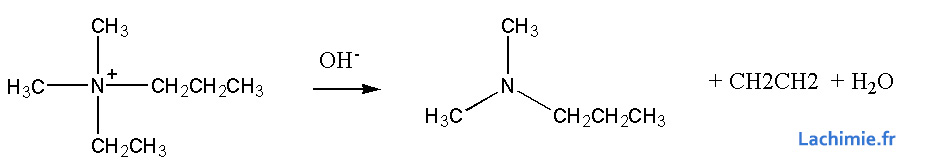
Réaction d'Hofmann
C'est une réaction délimination effectuées sur les ammonium quaternaire en milieu basique chaud. Elle conduit à la formation d'un composé éthylènique.
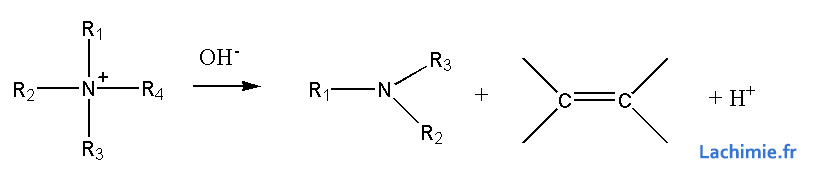
Si les groupements liés à l'azote sont différents, l'alcène formé sera celui obtenu à partir de la plus petite chaine carbonée. Par ailleurs, l'alcène le moins substitué sera majoritaire formé si plusieurs possibilités existent.