Isomérie : définitions et exemples
On appelle isomères des composés chimiques ayant la même formule brute mais dont les molécules sont différentes. Ces différences peuvent provenir soit de leur enchaînement d'atomes, soit de la disposition spatiale de ces derniers.
Isomérie de constitution ou fonctionnelle
C'est le cas le plus général de l'isomérie. Les enchaînements atomiques sont différents d'une molécule à l'autre. La formule semi-développée permet de les différencier. Par exemple pour une formule brute C4H8O, on peut avoir :
- Une cétone : la butanone
- Un aldéhyde : le butanal
- Un éther-oxyde : le THF
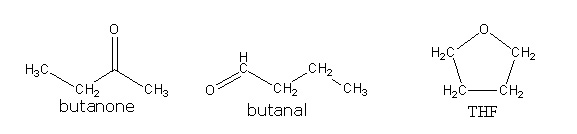
On distingue différents types d'isoméries de constitution :
Isomérie de position
Les groupements fonctionnels sont identiques mais n'occupent pas la même position sur la chaîne carbonée. C'est le cas par exemple du butan-1-ol et du butan-2-ol.
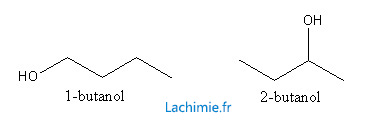
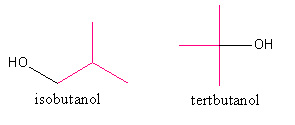
Isomérie de fonction
Les groupements fonctionnels de la molécule sont différents : un alcool et un éther oxyde par exemple (butanol et éther diéthylique).
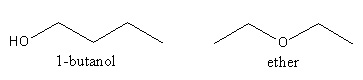
Toutefois, de nombreuses molécules ont les mêmes groupements fonctionnels placés sur les mêmes atomes de carbone, mais avec une disposition spatiale différente. Il faut alors s'intéresser à la stéréoisomérie des molécules.
Auteur de la fiche : Jean-Michel Riom